

Behandeling met rozanolixizumab leidt na 6 weken tot statistisch significante en klinisch relevante verbetering van de MG-ADL-score bij patiënten met gegeneraliseerde myasthenia gravis. Het bijwerkingenprofiel van deze remmer van de neonatale Fc-receptor was beheersbaar, waarmee het een goede toevoeging lijkt aan de bestaande behandelmogelijkheden. Tijdens EAN presenteerde prof. John Vissing (University of Copenhagen, Denemarken) de resultaten van deze fase III-studie.
Gegeneraliseerde myasthenia gravis is een zeldzame, chronische en onvoorspelbare auto-immuunaandoening. Deze ziekte wordt veroorzaakt door pathogene auto-antilichamen tegen componenten van de neuromusculaire junctie zoals de acetylcholinereceptor (AChR) en MuSK, dat zorgt voor clustering van de AChR. Een op de drie patiënten reageert niet op conventionele behandelingen, waardoor er nog altijd behoefte is aan aanvullende behandelmogelijkheden. Rozanolixizumab is een monoklonaal antilichaam dat gericht is tegen de neonatale Fc-receptor (FcRn). Rozanolixizumab, is een remmer van de FcRn. Dit leidt tot een versnelde afbraak van IgG, inclusief pathogene auto-antilichamen. In de MycarinG-studie werd rozanolixizumab onderzocht als behandeling van gegeneraliseerde myasthenia gravis.
In totaal werden 200 patiënten van 18 jaar of ouder gerandomiseerd (1:1:1) toegewezen aan placebo, rozanolixizumab 7 mg/kg (subcutaan, eenmaal per week), of rozanolixizumab 10 mg/kg (subcutaan eenmaal per week) voor een periode van 6 weken. Primair eindpunt van de studie was verandering van de MG-ADL-score (‘Myasthenia Gravis Activities of Daily Living’) vastgesteld op dag 43, waarna een observatieperiode volgde van 8 weken. Om in aanmerking te komen voor deelname, moesten patiënten bij aanvang een QMG-score (‘Quantitative Myasthenia Gravis’ score) hebben van ≥11 en een MG-ADL-score van ≥3, waarvan ten minste 3 punten non-oculair. Belangrijkste exclusiecriteria waren dat patiënten geen klinisch relevante infecties mochten hebben in verband met het uitlokken van een myasthene crisis , dat IgG-waarden ≤5,5 g/l waren en het aantal neutrofielen lager was dan 1500 cellen/mm3.
Patiënt- en ziektekenmerken bij aanvang van de studie waren goed in balans. Gedurende de behandelperiode van 6 weken nam de MG-ADL score geleidelijk af in de twee groepen die werden behandeld met rozanolixizumab. Dit resulteerde na 43 dagen tot een afname van gemiddeld 3,37 punten bij 7 mg/kg (n=66) en 3,48 bij 10 mg/kg (n=67) vergeleken met 0,78 punten in de placebogroep (n=67), overeenkomend met een least squares gemiddeld verschil van respectievelijk 2,59 (1,25-4,09; p<0,001) en 2,62 (1,16-3,99; p<0,001; zie Figuur 1).
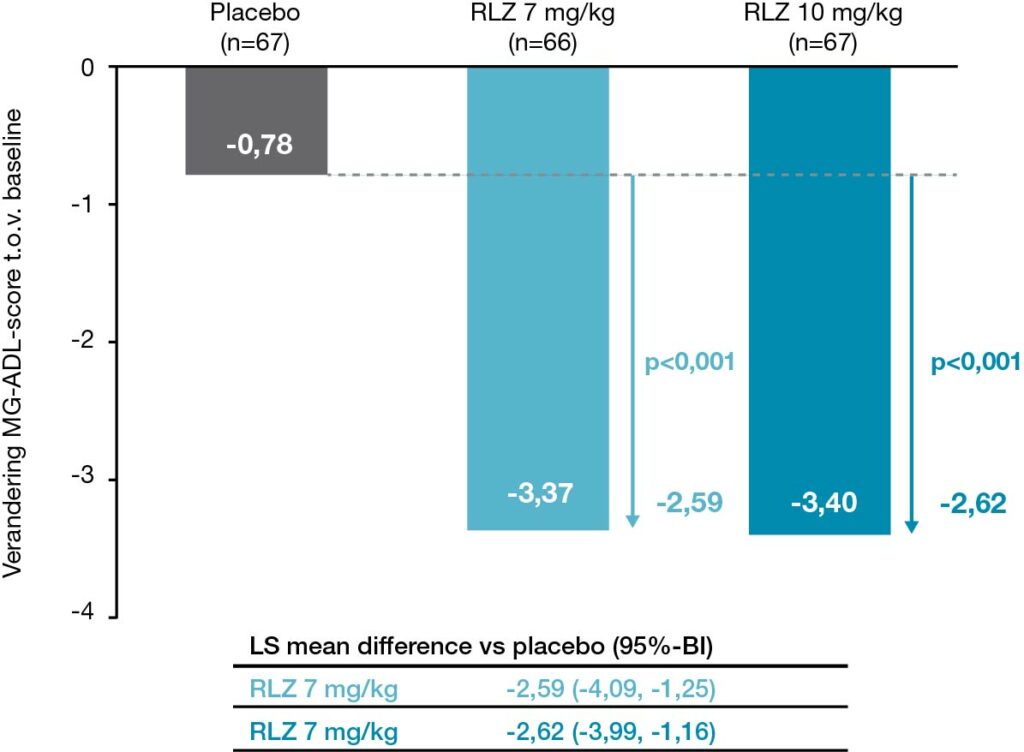
De onderzoekers keken vervolgens naar een aantal vooraf gedefinieerde subgroepen. Bij de populatie van patiënten van ≥65 jaar was sprake van minder herstel van de MG-ADL-score, maar dit gold voor alle drie de onderzoeksgroepen. De onderzoekers vonden geen verschil in effect op basis van geslacht, aanwezigheid van AChR- dan wel MuSK-antilichamen, ziekteduur, MGFA-klasse bij aanvang, en het wel of niet hebben gehad van een thymectomie.
In de twee onderzoeksgroepen die waren behandeld, was sprake van meer behandelingsgerelateerde bijwerkingen (53%) dan in de placebogroep (33%). De meest voorkomende bijwerkingen waren hoofdpijn en pyrexie. Het aantal ernstige bijwerkingen was vergelijkbaar in de drie groepen met 9%, 8% en 10% bij respectievelijk placebo, 7 mg/kg, en 10mg/kg.
De verbeteringen van MG-ADL scores vanaf baseline in beide rozanolixizumab groepen was klinisch relevant en statistisch significant. Verbeteringen werden gezien in alle onderzochte subgroepen. Het bijwerkingenprofiel van rozanolixizumab was beheersbaar en het wordt over het algemeen goed verdragen. Daarmee lijkt rozanolixizumab een goede behandeloptie voor patiënten met gegeneraliseerde myasthenia gravis.
Referentie
Vissing J, et al. Efficacy of rozanolixizumab in generalised myasthenia gravis: subgroup outcomes in the randomised phase 3 MycarinG study. Gepresenteerd tijdens EAN; late breaking news 1-2.