Editor’s pick van drs. Aline Delva, ASO neurologie, UZ Leuven
Momenteel wordt bij patiënten met relapsing-remitting multiple sclerose (RRMS) veel gebruik gemaakt van ziektemodulerende therapieën (‘disease-modifying therapies’) om zo ziekteactiviteit te verminderen.1 Voor de progressieve fase die vaak op RRMS volgt, of voor de primair progressieve vorm van de ziekte, was lange tijd geen medicamenteuze behandeling beschikbaar. Sinds korte tijd zijn siponimod en ocrelizumab geregistreerd voor respectievelijk actieve secundair progressieve MS en primair progressieve MS.2,3
Een behandeling die daarnaast al langere tijd wordt onderzocht voor MS-patiënten is de hematopoëtische stamceltransplantatie (HSCT). Deze therapie is in Nederland nog niet beschikbaar voor MS-patiënten. Wel is er al veel onderzoek gedaan naar de werkzaamheid van HSCT in studieverband. In 2017 werd een meta-analyse gepubliceerd waarin alle onderzoeken tussen 1995 en 2016 naar HSCT bij MS (ongeacht de vorm) werden geanalyseerd. In januari 2021 werden daarnaast de uitkomsten gepresenteerd van een observationele studie waarin MS-patiënten een stamceltransplantatie ondergingen en tot 11 jaar werden gevolgd.4
De meta-analyse includeerde 15 studies met totaal 764 patiënten die een transplantatie waren ondergaan.1 In de oudere studies bleek het aantal transplantatiegerelateerde overlijdens significant hoger te zijn (p=0,014), met een gepoolde overlijdensschatting van 2,1% (95%-BI: 1,3-3,4%) over alle studies. Daarnaast was het aantal transplantatiegerelateerde overlijdens positief gecorreleerd met een hogere EDSS-score (‘Expanded Disability Status Scale’) bij baseline (p=0,013).
Na 2 jaar was ziekteprogressie ontstaan bij 17,1% (95%-BI: 9,7-24,5%) van de MS-patiënten en na 5 jaar was dit het geval bij 23,3% (95%-BI: 16,3-31,8%). Wanneer een studie relatief meer RRMS-patiënten includeerde bleek de ziekteprogressiefrequentie lager te zijn (p=0,004). Verder waren er geen tekenen van ziekteactiviteit (‘No Evidence of Disease Activity’, NEDA) bij 83% (tussen 70-92%) van de patiënten na 2 jaar. Na 5 jaar was NEDA aanwezig bij 67% (tussen 59-70%).
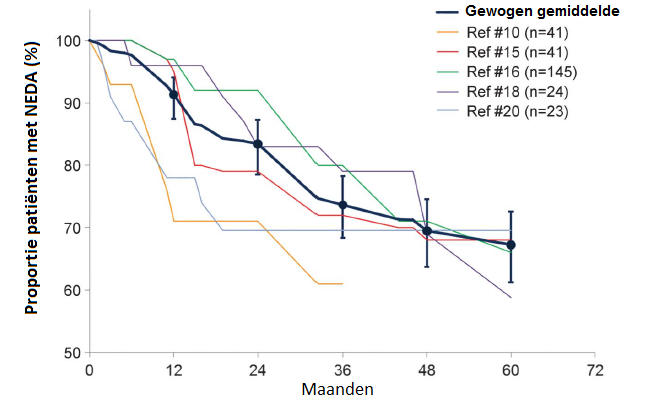
Uit deze analyse concludeerden de onderzoekers dat het grootste voordeel met HSCT te behalen valt bij patiënten met agressieve MS met een relapsing-remitting-ziekteverloop en waarbij nog geen grote invaliditeit wordt gezien.
Een nieuwe studie, gepubliceerd in Neurology, heeft daarnaast nieuwe inzichten verschaft over de langetermijneffectiviteit van HSCT bij het induceren van duurzame remissies. De studie includeerde 210 MS-patiënten waarvan 58% RRMS-patiënten. De mediane EDSS-score was 6 en de gemiddelde follow-up was 6,2 (±5) jaar.
Vijf jaar na de HSCT leefde nog 85,5% (95%-BI: 76,9-94,1%) van de RRMS-patiënten zonder verslechtering van de ziekte (‘disability worsening-free survival’). Na 10 jaar was dit het geval bij 71,3% (57,8-84,8%) van de RRMS-patiënten. Bij patiënten met progressieve MS was de overleving zonder ziekteverslechtering 71,0% (95%-BI: 59,4-82,6%) na 5 jaar. Tien jaar na de transplantatie leefde nog 57,2% (41,8-72,7%) van de patiënten met progressieve MS zonder ziekteverslechtering. Bij RRMS-patiënten nam de EDSS-score daarnaast significant af na het ontvangen van een stamceltransplantatie; gemiddeld met -0,09% per jaar (95%-BI: -0,15 tot -0,04%; p=0,001).
De onderzoekers concludeerden dat een HSCT ziekteprogressie kan voorkomen bij het merendeel van MS-patiënten. Zowel RRMS-patiënten als patiënten met een progressieve ziekte kunnen hier baat bij hebben. De remissies bleken ook duurzaam tijdens de follow-upperiode tot 11 jaar.4 In combinatie met de bevindingen uit de meta-analyse met kortetermijnresultaten van HSCT, lijkt HSCT een veelbelovende optie voor MS-patiënten met een agressieve ziekte, met zowel een progressief als relapsing-remitting ziekteverloop, waarbij de effectiviteit ook op langere termijn aanhoudt.
Referenties