
Van transcraniële gelijkstroomstimulatie (‘transcranial direct current stimulation’, tDCS) van de linker dorsolaterale prefrontale cortex is aangetoond dat dit tijdelijk het bewustzijnsniveau kan verbeteren bij patiënten met ernstig hersenletsel met bewustzijnsstoornissen. Dit is nu ook onderzocht in een grootschalige studie, waarbij de werkzaamheid ook is bevestigd bij specifieke subgroepen. Tijdens EAN werden de resultaten van deze sham-gecontroleerde studie gepresenteerd door dr. Aurore Thibaut (University Hospital of Liège, België).
Patiënten met een bewustzijnsstoornis (‘disorders of consciousness’, DOC) raken in comateuze toestand vanwege een ernstig hersenletsel door een hartstilstand, ernstig hersentrauma (‘traumatic brain injury’, TBI) of beroerte. Bij coma is geen sprake van het openen van de ogen en is het gedrag uitsluitend reflexmatig. Daarna komen patiënten terecht in wat voorheen als vegetatieve toestand werd omschreven, maar tegenwoordig niet-responsief waaksyndroom (NWS) wordt genoemd. Dat is een toestand waarbij patiënten de ogen openen (hetzij spontaan of door externe stimuli) maar het gedrag nog altijd uitsluitend reflexmatig is. Deze toestand kan maanden tot jaren achtereen in stand blijven. Sommigen ontwikkelen een geringe mate van bewustzijn, die als minimaal bewuste toestand (‘minimally conscious state’, MCS) wordt aangeduid. Bij MCS+ is sprake is van een hoger bewustzijnsniveau dan bij MCS- en is iemand in staat om verbale aanwijzingen op te volgen. Bij MCS- is de patiënt alleen in staat is om te volgen met de ogen of pijnprikkels te lokaliseren. Patiënten die ontwaken uit de MCS en in staat zijn om functioneel te communiceren en simpele objecten te hanteren, worden niet langer als DOC beschouwd. Voor DOC-patiënten bestaan geen opties voor actieve rehabilitatie. tDCS is een niet-invasieve benadering waarbij gebruik wordt gemaakt van twee of meer electroden met een zwakke elektrische stroom van 1-2mA die leidt tot neuronale excitatie met korte- en langetermijneffecten. tDCS geldt als veilig en vereist geen actieve deelname van de patiënt. Tot op heden ontbrak een grootschalig onderzoek, waarmee de werkzaamheid van tDCS wordt bevestigd.
In deze sham-gecontroleerde dubbelblinde gerandomiseerde studie werd onderzocht of het bewustzijn of reactievermogen van patiënten met een langdurige bewustzijnsstoornis tijdens hun revalidatie wordt verbeterd na 4 weken tDCS. tDCS van de linker dorsolaterale prefrontale cortex (LDLPFC) werd toegepast gedurende 20 dagen (vijf dagen per week). Er werd wekelijks gebruik gemaakt van de Coma Recovery Scale-Revised (CRS-R) gedurende een follow-up van 3 maanden. Het gedrag werd beoordeeld met gebruik van een lineair gemengd model. Daarmee werden gedragsveranderingen (na 4 weken en 3 maanden) vergeleken tussen de actieve tDCS-groep en de shamgroep. Verschillen bij week 4 en maand 3 ten opzichte van baseline werden beoordeeld met een Mann-Whitney test (zie Figuur 1).
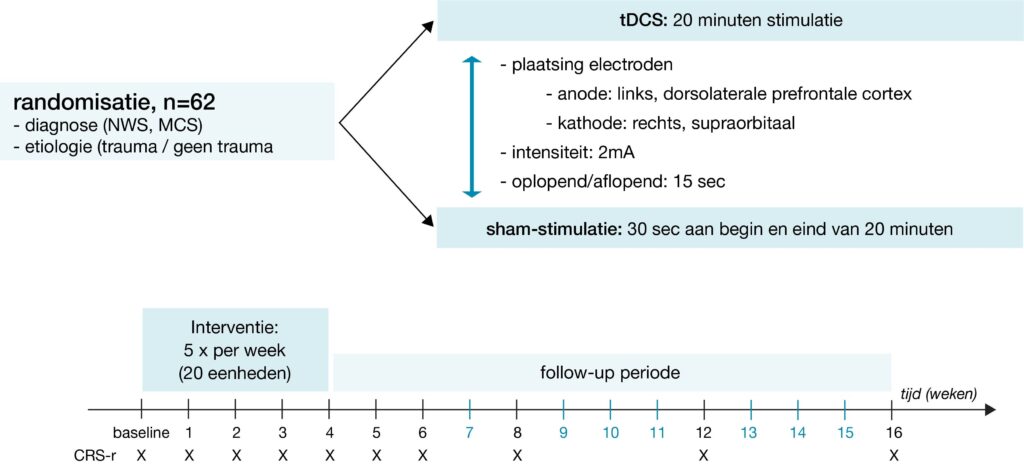
62 patiënten (waarvan 18 vrouwen, 30 MCS, 39 niet-TBI) werden 260 ±171 dagen na hun letsel behandeld (waarvan 33 met actieve tDCS) zonder enige ernstige bijwerkingen. In de totale populatie werd geen behandeleffect gevonden. Met subgroepanalyse werd echter een significante verbetering gevonden in de actieve tDCS-groep in vergelijking met de shamgroep bij patiënten met MCS (p=0,015) en TBI (p=0,023). In geen van de overige vergelijkingen werden significante verschillen gevonden.
De resultaten uit deze studie wijzen uit dat actieve tDCS tijdens de revalidatie in het algemeen niet leidt tot significante verbetering van tekenen van bewustzijn. Na 3 maanden follow-up was in de subgroepen van MCS- en TBI-patiënten echter wel een significant beter herstel te zien in de actieve tDCS-groep ten opzichte van de shamgroep. Daarom adviseren de onderzoekers om tDCS specifiek toe te passen in deze subgroepen van patiënten om hun revalidatie te bevorderen.
Referentie
Thibaut A, et al. Transcranial direct current stimulation for patients with disorders of consciousness: a multicenter randomized double-blind sham-controlled clinical trial. Gepresenteerd tijdens EAN 2022; abstract OPR-094.